それらの論考を載せる前に、その内容から小生なりにこの「リチウム・空気電池」を概略する。正しく内容を表現しているかは保証できないが、次のようになる。
(1)先ず電池であるからして、電解質を挟んで負極と正極がある。負極が金属リチウムで正極が空気である、といっても小生のような素人には正しくイメージ出来ないのだが、正極はどうも酸素を含みやすい(通しやすい)炭素材料などを使うようだ。
(2)負極の金属リチウムのリチウム原子から電子が放出され電流となり正極へ移動する。電子を失ったリチウム原子はリチウムイオンとなり、電解質を通って正極に移動する。これが「放電」である。
(3)正極に移動したリチウムイオンは、大気由来の酸素と反応して、酸化リチウムLi2Oとなり堆積する。
Li2Oが正極の炭素材料(の細孔)に蓄積し目詰まりとなり反応が停止してしまうため、炭素材料に酸化物触媒をくっつけて水溶電解液(アルカリ性の水溶性ゲル)と組み合わせるなどの方法が考案されている。
(4)以上が「放電」であるが、「充電」は、この酸化リチウムが酸素を大気に放出してリチウムイオンと電子となり、リチウムイオンは電解質を通って負極に戻り電子は導線を通して負極に戻り、そこでリチウムとなり蓄積される、という過程で進むということらしい。
参照論考①「IBM、電気自動車用リチウム空気電池を開発中。1回充電で走行距離800キロめざす」(http://sustainablejapan.net/?p=1248)
参照論考②「次世代二次電池の研究成果」(http://www.toyota.co.jp/jpn/tech/environment/next_generation.html)
参照論考③「新しい構造の高性能「リチウム-空気電池」を開発(産総研)」
http://www.aist.go.jp/aist_j/press_release/pr2009/pr20090224/pr20090224.html
このため理論的には、何らかの方法をとれば、放電と充電を繰り返すことが出来そうだ。また負極の金属リチウムをその都度供給し正極の多孔質炭素を入れ替えれば、放電は理論的には続けられるという。燃料電池の場合は、この金属リチウムが水素に置き換わっているのである。だから水素が継続的に供給され酸素と結びついてゆけば、燃料電池は発電し続けるように、理論的には金属リチウムが供給され続けて正極からも酸素が供給され続ければ、「金属リチウム・酸素電池」は発電し続けるのであろう。
Wikipediaによれば、この動きは「燃料電池」と同じであると言う。
燃料電池とは次のような反応である。
(1)負極に水素H2を供給する。
(2)H2は電子を放出して水素イオンとなる。H2→2H++2e-
(3)電子2e-は正極に移動する(放電)。電気が発生する。
(4)水素イオン2H+は高分子電解質膜を通り正極へ移動する。
(5)正極では2H+と2e-と、空気中の1/2O2と結合して水H2Oとなる。
このH2をリチウムLiに置き換えれば、リチウム・空気電池と同じ様子となる。だからリチウム・空気電池は一種の燃料電池といってもよいのである。
そしてこのリチウム・空気電池の性能は、リチウムイオン電池の5,6倍以上の電池性能を持っているといわれている。だから電気自動車の電池として有望視されているのである。
ということの様であるが、次に参照した論考を掲載する。
新しい構造の高性能「リチウム-空気電池」を開発(産総研)
発表・掲載日:2009/02/24
・・・・・・
研究の経緯
産総研エネルギー技術研究部門では、次世代「リチウムイオン電池」を目指して、電極材料をナノ構造化することで、大出力化が期待できることを示してきた(2005年1月18日、2007年11月19日、2008年8月27日産総研プレス発表)。自動車用にはさらなる大幅なエネルギー密度のアップが必要となるので「リチウム-空気電池」の研究も精力的に進めてきた。
従来のリチウム-空気電池の問題点
1)正極に固体の反応生成物(Li2O)が蓄積し細孔を目詰まりさせ、放電が止まる。
2)空気中の水分が金属リチウムと反応すると危険な水素ガスを発生する。
3)空気中の窒素が金属リチウムと反応して放電を妨害する懸念がある。
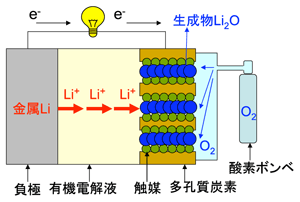
図1 従来のリチウム-空気(酸素)電池の原理図
産総研では、従来の電池の問題点を踏まえ、負極側に金属リチウムと有機電解液、正極側に空気極と水性電解液、両電解液の隔壁として固体電解質に着目し研究開発を行ってきた。